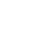肝纖維化的分子成像進展
發布時間:2019-04-19作者:洛陽慈銘健康管理有限公司點擊:4106 次
肝纖維化是各種慢性肝損傷的共同轉歸。肝星狀細胞(hepatic stellate cell,HSC)在損傷因素作用下活化并分泌過量細胞外基質(extracellular matrix,ECM),使纖維合成與降解比例失衡,大量膠原纖維在肝內沉積,即為肝纖維化。早期診斷肝纖維化并積極干預具有重要臨床意義。超聲、CT、常規MRI等傳統影像技術主要著眼于形態學變化,對早期肝纖維化敏感性不高。
功能成像如超聲瞬時彈性成像、MR彈性成像(magnetic resonance elastography,MRE)和擴散加權成像(DWI)等有助于肝纖維化的診斷及評估,但研究的參數均為肝纖維化進展到一定階段表現出的間接指標,易受炎癥、淤血、脂肪沉積等因素影響。肝纖維化分子成像基于病程中異常表達的靶分子,利用能與其特異性結合且能被影像監測的分子探針,在真實完整的生理環境中通過影像直接觀察細胞和分子通路,對病變的發生、發展過程進行成像,有利于早期診斷肝纖維化、協助靶向藥物研發、監測治療療效等。本文就目前已知的主要生物靶點闡述肝纖維化分子成像研究進展。
1.aHSC相關靶點
HSC激活后轉化為活化的肝星狀細胞(activated hepatic stellate cell,aHSC)是肝纖維化發生、發展的核心環節,故aHSC是肝纖維化診斷及治療的重要靶點。
1.1整合素αvβ3
整合素是由α、β兩個亞單位構成的異親性細胞粘合二聚體糖蛋白。肝纖維化進程中aHSC膜表面表達的整合素αvβ3顯著增多,且aHSC是表達整合素αvβ3的主要細胞類型,αv和β3亞基的表達量與肝纖維化程度密切相關。精氨酸-甘氨酸-天冬氨酸(argininel-glycine-asparagic,RGD)序列是可與αvβ3結合的特異性配體,兩者具有很強的親和力和靶向性。
Wang等研發了RGD多肽偶聯的超小超順磁性氧化鐵(ultrasmall superparamagnetic iron oxide,USPIO)探針RGD-USPIO,可特異地顯示肝纖維化時活化的HSC,為肝纖維化的診斷提供了一種基于分子水平的有效方法。進一步研究證實,隨肝纖維化的進展,整合素αvβ3的表達水平增高,RGD-USPIO與aHSC間特異性結合增加,各期肝纖維化之間ΔR2*差異具有統計學意義,且T2弛豫率變化與肝纖維化程度呈負相關,可用于肝纖維化早期診斷與分級。
樹枝狀聚合物(dendrimers,Den)是一種高度支化且具有特定三維結構的納米級分子。Li等將釓特酸葡胺(Gd-DOTA)、RGD環肽連接在此高分子上,組成靶向aHSC的納米探針。與單體Gd-DOTA相比,該探針將大量的成像基團連接到同一個納米粒上,能顯著放大T1加權信號。99Tcm-3P-RGD可用于單光子發射計算機體層成像(SPECT)及SPECT/CT成像。
通過該探針可探測纖維化肝臟aHSC中整合素αvβ3表達的升高,對肝纖維化進行診斷與定量分析,以30min時影像上肝臟與心臟興趣區(ROI)的放射性計數比值作為肝臟攝取99Tcm-3P-RGD的定量評價指標。肝臟99Tcm-3P-RGD的濃聚與肝纖維化的進展及硫代乙酰胺(thioacetamide,TAA)的暴露時間成正比,與膠原比例面積、Ishak分級評分具有良好相關性。
Guo等將此探針與131I-新半乳糖白蛋白探針合用,較單模態探針能更有效地評估肝臟的結構和功能。但SPECT檢測敏感度相對較低、分辨力較差。99Tcm-3P-RGD探針主要通過腎臟排泄,腎內濃聚大量放射性藥物且右腎與肝臟在冠狀面成像中部分重疊,易影響肝纖維化的評估。PET/CT成像具有更高的探測敏感度,采用18F-FDG-RGD能夠提高RGD多肽的親水性和肝臟影像質量,降低了血液本底,在肝纖維化定量評估中有明顯優勢。
有研究者將熒光基團、Gd-DOTA、RGD環肽連接到第5代Den上,成功合成了帶有磁性、光學成像基團的雙模態納米探針,該探針可特異、敏感地與肝纖維化組織迅速、大量結合,并潴留一定時間。MRI具有高分辨力,可對深部組織進行準確定位、定量分析,但其敏感性較低;光學分子成像具有高敏感度,但其成像深度有限;熒光成像與MRI融合成像,兩者可優勢互補。
基于RGD肽的分子探針是當前分子成像研究的熱點,在肝纖維化的診斷、治療及預后評估中具有良好前景,但肝纖維化與肝慢性炎癥、肝癌病理表現存在重疊。肝內有慢性炎癥時會有新生血管形成,整合素αvβ3在肝癌的腫瘤組織血管內皮也高度表達,今后可進一步優化該探針的診斷特異性。
1.2轉位分子蛋白
HSC活化時,其線粒體外膜上的18ku轉位分子蛋白(translocator protein,TSPO)表達上調。特異性靶向TSPO的PET探針18F-FEDAC的放射性分布與TSPO的表達密切相關,肝放射性攝取值的增加與肝纖維化程度成正比,可用于肝纖維化的診斷和分級。
1.3波形蛋白和結蛋白
隨肝纖維化的進展,HSC細胞中波形蛋白與結蛋白的表達上調。N-乙酰氨基葡萄糖(N-acetylglucosamine,GlcNAc)是靶向波形蛋白和結蛋白的特異性糖配體。GlcNAc與吲哚菁綠(indocyaninegreen,ICG)、聚乙烯亞胺(PEI)/TGFβ1siRNA制成的PEI-D-GlcNAcICG/siRNA探針對波形蛋白、結蛋白有較好的靶向性,能選擇性濃聚在肝纖維化區域,結合siRNA的干擾效果,可用于肝纖維化顯像及治療。
2.ECM相關靶點
肝纖維化進程中ECM(如纖維膠原蛋白、糖蛋白、黏多糖等)分泌增加,降解減少,在肝內大量沉積并形成交聯,是肝纖維化的病理基礎。分子成像可直接反映活體內ECM的分布、密度與功能,為肝纖維化的準確診斷與有效治療提供更多信息。
2.1Ⅰ型膠原蛋白
肝纖維化進程中Ⅰ型膠原蛋白的量顯著增加,是監測肝纖維化的重要靶標。EP-3533由16個氨基酸分子加3個Gd-DTPA螯合劑分子合成,能與Ⅰ型膠原蛋白特異性結合,其濃聚程度與肝內羥基脯氨酸(膠原成分)含量呈線性相關,可用于肝纖維化分期。該探針在低場強MRI和治療后模型均表現出良好的診斷效能,圖像縱向弛豫速率變化值(the change in longitudinal relaxation rate,△R1)可量化評價探針特異性濃聚。
有研究將EP-3533分子成像與MRE結合,分子成像對早期病變敏感,MRE對晚期肝纖維化敏感度高,兩種技術互補,有效提高了診斷準確性。Chilakamarthi等將膠原結合肽與5-(4-羧基苯)-10,15,20-三苯基卟啉結合,合成了靶向Ⅰ型膠原蛋白的卟啉類近紅外熒光探針化合物。此探針具有良好近紅外熒光特性,較強的纖維靶向性,在無關組織中的聚集較少,具有良好的診斷特異性。
2.2纖維蛋白原-纖維連接蛋白復合物
纖維連接蛋白是一種存在于肝臟ECM中的糖蛋白。肝纖維化進程中,纖維蛋白/纖維蛋白原與纖維連接蛋白交聯,纖維蛋白原-纖維連接蛋白復合物顯著增加。小分子多肽CLT1可定向結合腫瘤或瘢痕組織中纖維蛋白-纖維連接蛋白復合物,且不與正常組織中的類似物質結合。由環狀十肽、CLT1多肽、Gd-DTPA連接制成CLT1-(Gd-DTPA)探針,對肝纖維化模型中的纖維蛋白-纖維連接蛋白復合物具有較強的靶向性,可用于肝纖維化診斷、分級。但該探針體分子質量大、所需劑量大,在體內代謝較慢,臨床應用受限,需進一步優化,增強診斷敏感性及特異性。
2.3彈性蛋白
彈性蛋白屬于ECM中非膠原蛋白類。隨肝纖維化進展,彈性蛋白比膠原蛋白比值增加。ESMA(BMS-753951)是一種靶向彈性蛋白的低分子質量新型對比劑,由釓螯合物與苯基苯丙氨酸相連。成像時,纖維化區域可見明顯局灶性強化而健康肝臟無異常強化。彈性蛋白多表達于肝纖維化后期,ESMA診斷早期肝纖維化敏感性不高,有望用于監測抗肝纖維化治療療效。
3.肝細胞膜去唾液酸糖蛋白受體(asialoglycoprotein receptor,ASGPR)
ASGPR是一種異源低聚物內吞受體,主要位于竇狀隙一側的肝細胞膜表面。當有肝炎、肝纖維化或肝癌時,其數量和活性均受損,可用于定量評估肝儲備功能。18F-FBHGal為特異性靶向ASGPR的單價半乳糖衍生物,在纖維化肝臟中濃聚量顯著低于正常肝臟。
靶向ASGPR的SPECT探針99Tcm-p(VLA-co-VNI)攝取值與肝臟羥脯氨酸呈負相關。半乳糖血清白蛋白(GSA)與68Ga偶聯用于PET顯像,能準確區分早期和中期肝纖維化。此類探針在評價肝儲備功能中有獨特優勢,但對肝纖維化診斷特異性稍差。
4.其他
肝組織毛細血管和肝細胞水通道蛋白(aquaporins,AQP)的數量、分布及功能隨肝臟纖維化的進展而變化。Han等采用13N-NH3H2O評估AQP,能檢出早期纖維化時的功能受損。生長因子是促進肝纖維化最有力的細胞因子,有研究團隊[制備了靶向生長因子的人工microRNA超聲微泡對比劑,運用超聲靶向破壞微泡(ultrasound targeted microbubble destruction,UTMD)技術介導有關基因治療大鼠肝纖維化。肝臟肌成纖維細胞(hepatic myofibroblast,HM)在肝纖維化過程中發揮重要作用,靶向HM的單鏈抗體C1-3與熒光基團相連制成的近紅外光光學探針,對HM表現出良好靶向性及敏感性,可用于診斷急性肝纖維化、監測療效,亦可作為載體用于抗纖維化的治療。
5.小結與展望
肝纖維化進程中有大量生物分子與疾病發展密切相關,尋找其機制中心環節的分子成像靶點是進一步開展工作的主要方向。一個優異的靶點需要滿足:①敏感性高:在肝纖維化組織中高表達。②特異性高:病變組織與正常組織明顯差異性表達(TSPO在正常肝Kuffer細胞中可為陽性,診斷特異性不高)。③易接近:靶向胞質蛋白或核蛋白需克服細胞膜的限制,而膜表面靶點分子具有易接近、易識別等優點,故膜表面分子是肝纖維化中首選靶點分子。因此,整合素αvβ3和Ⅰ型膠原蛋白是肝纖維化早期診斷中優異的靶點,RGD多肽分子質量小、體內穩定和低免疫源性使靶向αvβ3的RGD探針更具優勢。
肝纖維化的分子成像發展迅速,磁性納米粒子、放射性核素等信號分子也可發揮治療作用,目前的研究方向主要為制備多模態探針及診療一體化探針。基于不同影像技術的分子成像各具優勢,但也存在自身難以克服的缺點和局限,尚沒有一種技術能同時提供檢測對象所有的結構、功能和病理信息,故可同時被多種影像手段探測到的多模態分子成像技術擁有廣闊的應用前景。但不同成像模態的敏感性相差巨大(如MRI與PET的敏感性可相差3個數量級以上,MRI探針的需要量要遠遠大于PET探針)。
理想的多模態探針并不是將兩種單一探針簡單相加,如何調整兩種探針的比例需要進一步探索和研究。目前肝纖維化的發生、發展和修復的機制仍在完善中,且臨床上肝纖維化致病因素多樣,不同致病因素導致的肝纖維化病人中異常分子的表達量及其與肝纖維化分級分期之間關系仍需要進一步研究。肝臟內含多種細胞,其中Kuffer細胞、竇狀內皮細胞、肝細胞等均可非特異性攝取分子探針,造成背景噪聲偏高,因此分子探針的制備及運用需注重上述問題。相信隨著肝纖維化的特異性標志物不斷的探索與發現,多模態探針合成技術的不斷提高,肝纖維化的分子成像將更具應用前景。
- 下一篇:常用治療痛風的藥物有哪些副作用?



 豫公網安備 41030502000297號
豫公網安備 41030502000297號